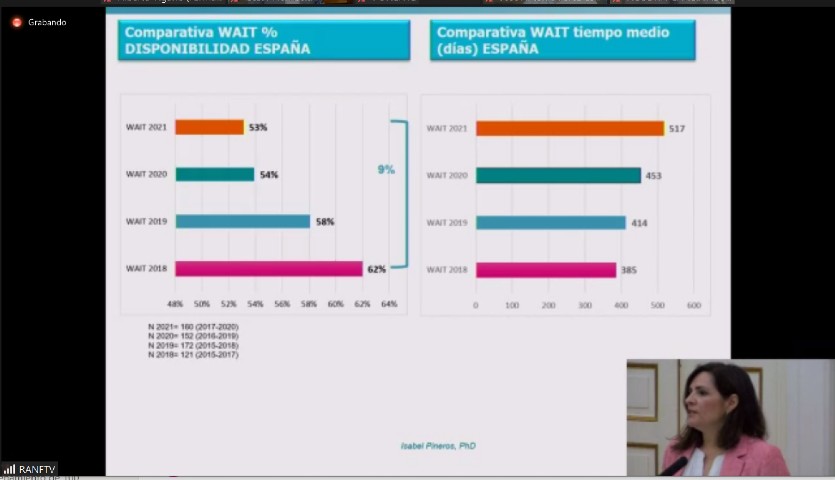
La inversión en nuevos medicamentos es el mayor responsable de que las personas cada vez vivan más años. En las últimas dos décadas se han producido grandes logros en la medicina que se han traducido en importantes incrementos de la esperanza media de vida. Sólo en la primera década de este siglo se ganaron 1,74 años de vida en los países desarrollados, de los que el 73% se puede atribuir directamente al efecto positivo de los nuevos medicamentos sobre la salud de la población. Así lo destacó este martes la directora del Departamento de Acceso de Farmaindustria, Isabel Pineros, en la Jornada de debate sobre acceso a la innovación farmacéutica: perspectivas en España y en la UE, celebrada en la Real Academia Nacional de Farmacia, dentro de la Cátedra GSK de Innovación Farmacéutica.
Esta apuesta constante por la investigación de la industria farmacéutica se ve reflejada en la aparición de nuevos tratamientos innovadores. De hecho, en 2021, en Europa se aprobaron 54 nuevos medicamentos, el récord de los últimos cinco años. Sin embargo, aseguró Pineros, buena parte de esta innovación no está llegando a los pacientes, lo hace con mucho tiempo de retraso o con restricciones, lo que se explica en gran medida por el proceso nacional de financiación. “En nuestro país son muchos los medicamentos y nuevas indicaciones que llegan autorizados desde Europa, pero el procedimiento español para fijar precio y financiación pública no da respuesta, ya que se ha hecho cada vez más lento e impredecible, lo que está provocando un importante retraso en el acceso de los pacientes a nuevos tratamientos”, apuntó.
Esta preocupación fue compartida también por el resto de los ponentes de la jornada: Inés Losa, de la junta directiva de la Plataforma de Organizaciones Pacientes (POP), y José Luis Fernández, director general de la consultora Iqvia España. Precisamente, el martes la Federación Española de Enfermedades Raras (Feder) denunciaba este mismo problema en una jornada celebrada en el Congreso de los Diputados, donde también participó Farmaindustria.
Mejoras en el procedimiento actual de financiación
Buena parte de esta falta de disponibilidad de los últimos tratamientos en España se debe, según Pineros, al funcionamiento del nuevo Plan de consolidación de los informes de posicionamiento terapéutico (IPT), el instrumento que el Ministerio de Sanidad puso en marcha para definir, con la evidencia científica disponible, la posición que el nuevo medicamento (o su nueva indicación) ocupa en el mercado en comparación con otros ya existentes y que, a su vez, sirviera para evitar evaluaciones sucesivas que se producen en la Administración sanitaria (comunidades autónomas y hospitales) tras la decisión de financiación. “Sin embargo, en la práctica, este instrumento no está contribuyendo a mejorar el acceso a los medicamentos, ya que ha supuesto una paralización del trámite de financiación mientras este informe se realiza, lo que está dilatando enormemente el periodo de aprobación”, explicó.
Abogó por adoptar criterios de evaluación y financiación específicos que miren más allá del coste-efectividad de estos medicamentos y tenga en cuenta el valor social de la innovación, un criterio establecido en la Ley de Garantías, subrayó. “Tenemos que avanzar en una mayor evaluación del valor social que supone la aprobación de muchos nuevos medicamentos, incluyendo los ahorros sanitarios y no sanitarios y el impacto sobre la productividad y el empleo, porque ahora tenemos las herramientas para poder medir ese valor”.
Otras mejoras para asegurar que todos los pacientes puedan acceder rápidamente a los mejores tratamientos farmacéuticos disponibles y que el sistema sanitario pueda financiarlos serían, entre otras, señaló Pineros, el establecimiento de un sistema de acceso temprano a aquellos tratamientos que aporten mayor beneficio; usar mecanismos específicos de precio y financiación para el tratamiento de las enfermedades raras; incluir a los clínicos y los pacientes en el proceso de financiación; utilizar la medición de los resultados en salud para resolver las incertidumbres percibidas por la Administración, o conseguir un seguimiento y mayor coordinación entre las comunidades autónomas para asegurar un acceso equitativo, ya que éstas forman parte del tercer escalón del acceso, que es clave para que la innovación llegue a los pacientes.
 | Innovamos para las personas
| Innovamos para las personas